陽電子断層撮像
核医学の画像診断技術の1つに、陽電子断層撮像(positron emission tomography; PET)があります。がんやアルツハイマーの診断に有効で、すでに実用化されている技術です。
PET診断ではベータプラス崩壊する放射性同位元素を含む薬剤を患者に投与し、患部に薬剤を集中させます。がんの場合だと、がん細胞は糖を消費する性質があるため、ブドウ糖に18-Fを付加するとがん細胞に18-Fが集まります。18-Fが崩壊すると陽電子が放出され、体内の電子と対消滅します。その際に2つ1組の511 keVガンマ線が反対方向に放出されるため、体の周囲を取り囲んだ検出器で検出します。検出器には、検出効率とコストの面からシンチレーション検出器が多くの場合で採用されています。
ペアのガンマ線が同時に検出される位置がわかると、その2点を結ぶ線上に放射源であるがん細胞があるはずです。多数の対消滅ガンマ線を観測し、結んだ線を重ね合わせていくとガンマ線発生源を画像が得られます。これがPETの基本的な原理です。
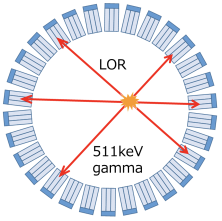
PETの撮像原理:対消滅ガンマ線を同時検出する
画質向上技術
Depth-of-Interaction (DOI)
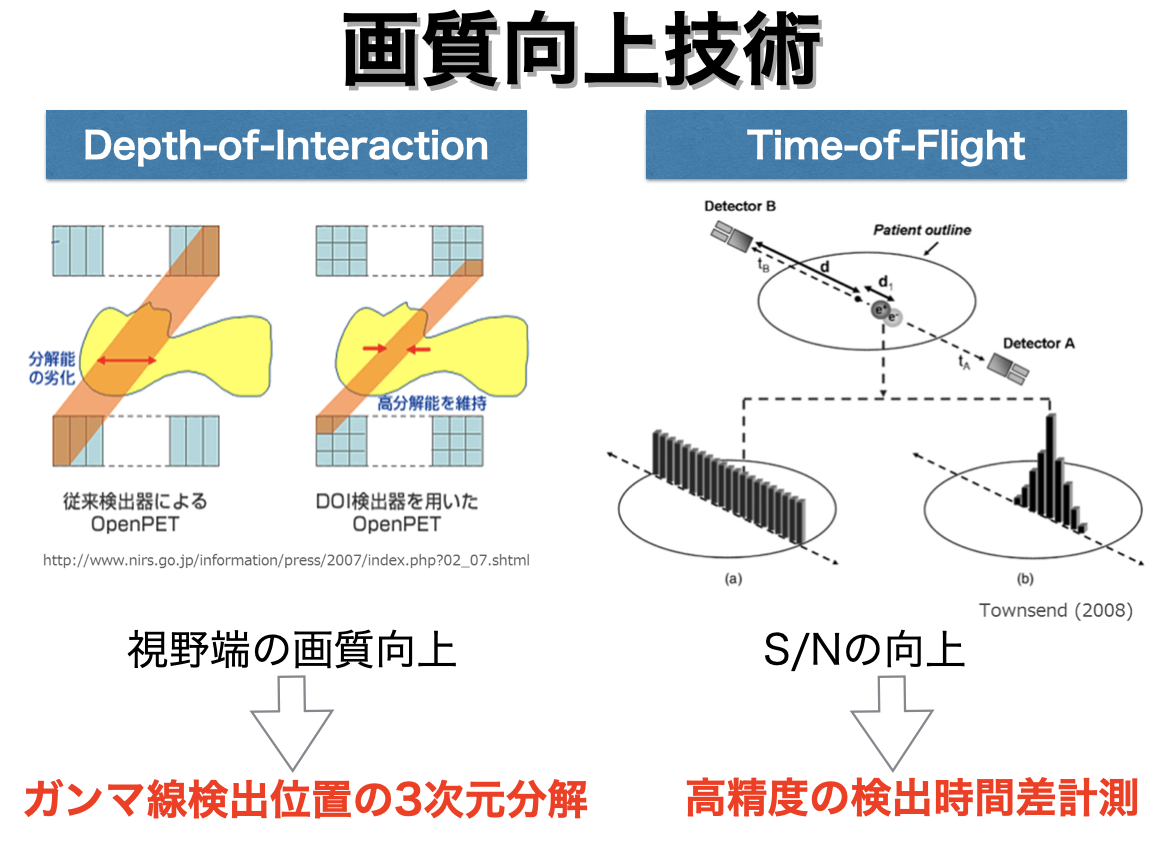
ガンマ線の検出位置は、シンチレータのピクセルの中のどこで反応したかを知ることは困難です。とくにシンチレータの深さ方向に反応位置(Depth-of-interaction;DOI)の分解能があると、端のシンチレータが吸収した際に、反応位置の推定精度が向上します。このようなPETはDOI-PETと呼ばれ、診断画像の分解能の向上が期待されます。
Time-of-flight (TOF)
対消滅ガンマ線の検出位置情報からは、2点を結ぶ線上のどこかに放射源がある、ということしかわかりません。この情報に加えて、2点の検出時間差を精密に測定すると、直線上の一部に放射源を絞り込むことができます。Time-of-flight (TOF) PETと呼ばれるシステムです。
TOF情報で放射線の範囲が制限できると、画像のS/N比が向上します。そしてより短時間で医学診断に必要な画像が得られます。すなわち、患者に投与する放射性薬剤の量を減らすことができ、患者の被ばく量を抑えることもできます。臨床の観点では患者の負担軽減は重要な要素です。
放射源を体内のがん組織の大きさにまで制限するためには、ナノ秒を切る時間計測精度が要求されます。ガンマ線の検出時刻の精度を決めるのは、ガンマ線と反応するシンチレータの応答タイムスケールと、検出時刻計測回路の性能です。
プラスチックシンチレータでTOF
プラスチックシンチレータの発光時定数は数ナノ秒で、従来PET装置に使われてきた高速の無機シンチレータ(例えばLYSO:Ce)などより1桁短い。プラスチックシンチレータをTOF-PETに採用できれば大幅な軽量化とコストダウンが期待できますが、原子番号と密度が小さいため光電吸収の断面積が小さく、検出効率が悪いと問題があります。しかし、コンプトン散乱を利用すれば検出効率を維持することができます。
そこで、図のようにプラスチックシンチレータを内側、無機シンチレータを外側に配置した2層構造のガントリを考えます。それぞれのシンチレータはDOIに対応した3次元位置分解を持たせると、内周のプラスチックを散乱体、外周の無機シンチレータを吸収体としたコンプトン型ガンマ線検出器になります。
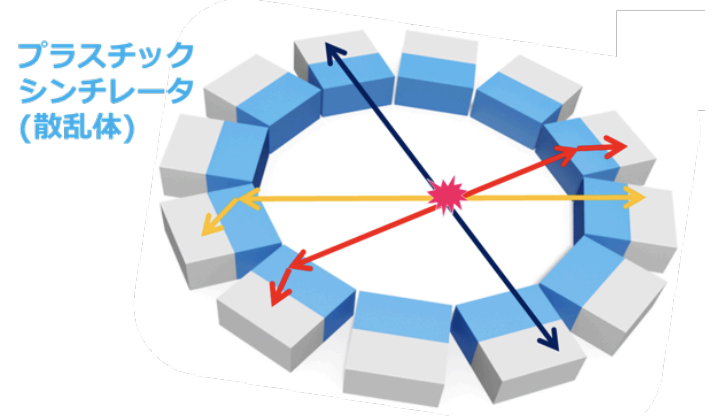
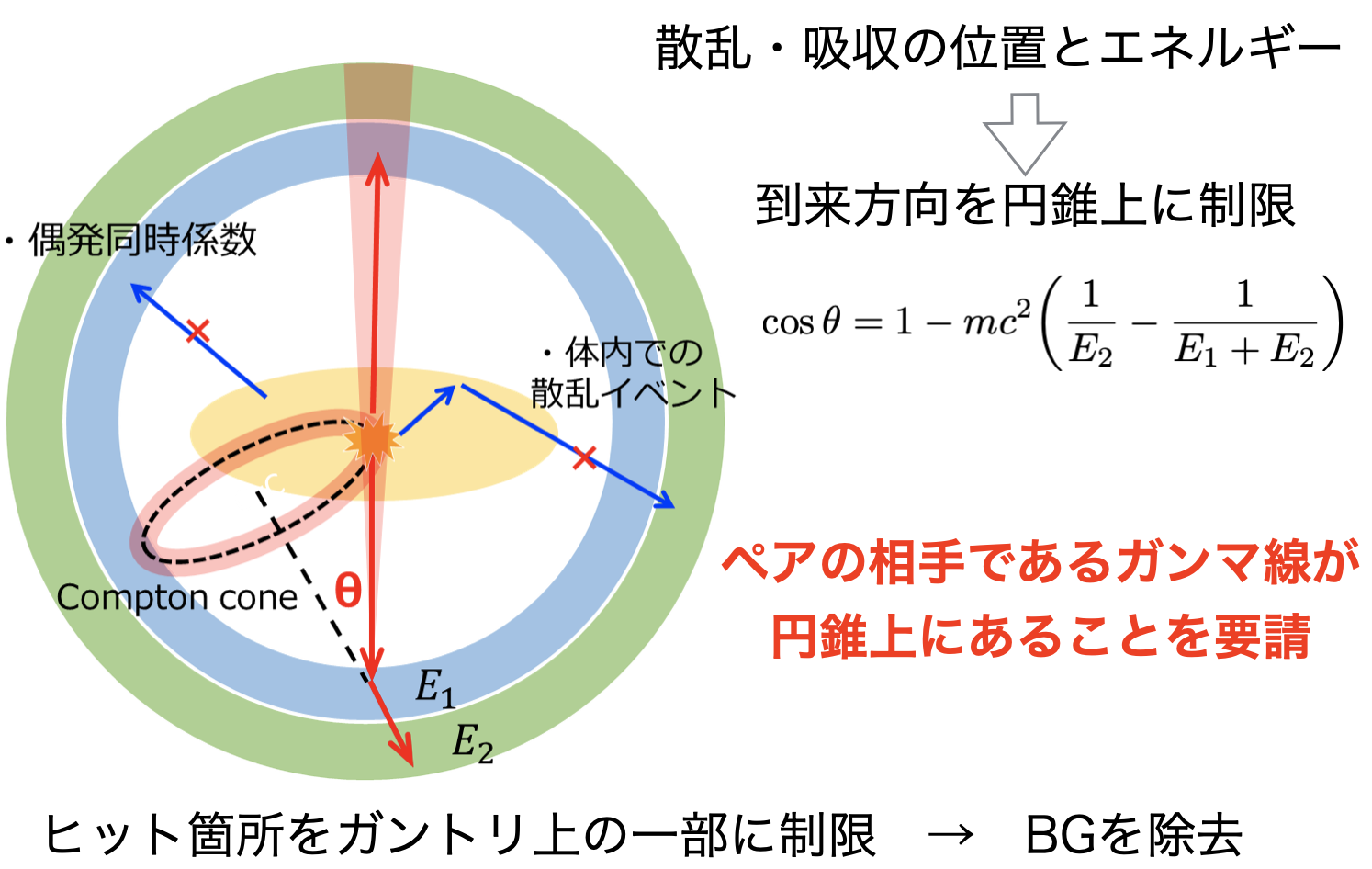
プラスチックではコンプトン散乱または透過、無機シンチレータでは光電吸収するケースの組み合わせでイベントを再構成します。対消滅ガンマ線ペアがそれぞれプラスチックで反応するとTOFも使えるという原理です。また、コンプトン散乱は到来方向を円環状に制限することができるため、偶発同時イベントなどの雑音事象を排除する能力も獲得します。